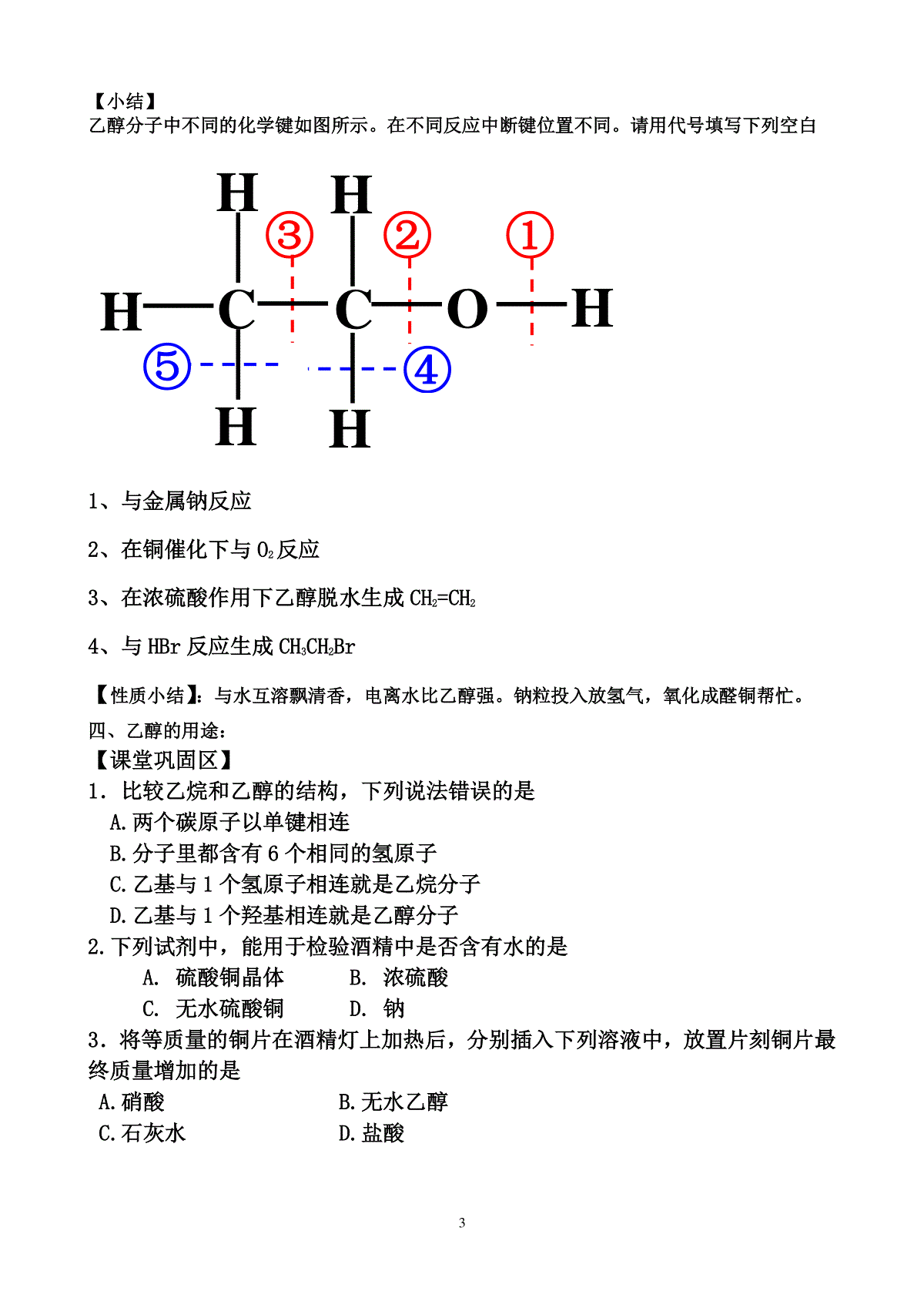
1第3节饮食中的有机化合物第一课时乙醇【学习目标】1、掌握乙醇的物理性质及其用途2、掌握乙醇的组成及主要化学性质:与活泼金属钠、氧化反应(燃烧和催化氧化)。3、通过实验的观察与分析,加强比较概括总结的能力。【教学重点】乙醇的化学性质。【教学难点】乙醇发生催化氧化反应和消去反应机理与规律。【课前预习区】阅读教材p76-78,思考1、乙醇的俗名分子式结构式结构简式2、乙醇的物理性质:乙醇是色味溶于水的体,沸点于水,与水互溶。医疗上消毒用的酒精是体积分数为的乙醇溶液。3、乙醇燃烧现象燃烧方程式4、钠与水反应的实验现象:。写出反应的化学方程式5、工业酒精能否饮用,为什么?【课堂互动区】一、乙醇的物理性质俗名,色通明、有特殊的液态,比水,易挥发,能与水,是优良的。医疗上消毒用的酒精是体积分数为的乙醇溶液。二.乙醇的结构:分子式结构式结构简式三.乙醇的化学性质:21、【实验探究一】实验现象化学方程式在烧杯中盛有2mL的无水乙醇,向试管中分别投入绿豆粒大小的金属钠,观察并记录实验现象。[问题组1](1)煤油与钠不反应,乙醇、水与金属钠能反应产生气体,说明什么问题?(2)下图是煤油、乙醇、水的分子结构式,仔细观察,回答问题:煤油乙醇水乙醇、水与金属钠反应速率和剧烈程度明显的不同,说明什么问题?【归纳总结】1、乙醇与金属钠的反应:①化学方程式:②金属钠沉在乙醇下面说明乙醇的密度比水。③反应的剧烈程度比水。说明乙醇中羟基氢比水中羟基氢活泼性。2、乙醇的氧化反应①燃烧反应:化学方程式:【实验探究二】分组实验向试管里注入约2mL无水乙醇,取一根光洁的铜丝绕成螺旋状,放在酒精灯外焰上加热,然后伸入无水乙醇中,反复几次。观察铜丝的变化并闻液体的气味。【归纳总结】②催化氧化实验现象:;化学方程式为;铜丝在总反应式中的作用是;理由是—3【小结】乙醇分子中不同的化学键如图所示。在不同反应中断键位置不同。请用代号填写下列空白1、与金属钠反应2、在铜催化下与O2反应3、在浓硫酸作用下乙醇脱水生成CH2=CH24、与HBr反应生成CH3CH2Br【性质小结】:与水互溶飘清香,电离水比乙醇强。钠粒投入放氢气,氧化成醛铜帮忙。四、乙醇的用途:【课堂巩固区】1.比较乙烷和乙醇的结构,下列说法错误的是A.两个碳原子以单键相连B.分子里都含有6个相同的氢原子C.乙基与1个氢原子相连就是乙烷分子D.乙基与1个羟基相连就是乙醇分子2.下列试剂中,能用于检验酒精中是否含有水的是A.硫酸铜晶体B.浓硫酸C.无水硫酸铜D.钠3.将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻铜片最终质量增加的是A.硝酸B.无水乙醇C.石灰水D.盐酸CCOH①③④⑤②HHHHH44.自2005年起,山东省就全面推广使用乙醇汽油作为发动机燃料,即汽油中掺入一定比例的乙醇,以代替一部分汽油。下列有关说法正确的是A.乙醇汽油是一种清洁能源,燃烧不会产生污染B.乙醇与汽油组成元素相同,化学成分相似C.乙醇汽油燃烧时,耗氧量高于等质量的汽油D.乙醇可通过淀粉转化制得,是一种可再生的燃料【课后练习】1.质量为ag的铜片在空气中灼烧变黑,趁热放入下列物质中铜丝变为红色,而且质量大于ag的是()A.硝酸B.无水乙醇C.澄清石灰水D.一氧化碳2.下列选项中说明乙醇作为燃料的优点的是①燃烧时发生氧化反应②充分燃烧的产物不污染环境③乙醇是一种再生能源④燃烧时放出大量热量A.①②③B.①②④C.①③④D.②③④*3.某有机物6g与足量钠反应,生成0.05mol氢气,该有机物可能是()A.CH3CH2OHB.C.CH3OHD.CH3—O—CH2CH34.用普通酒精制无水酒精的方法是()A.加入NaOH溶液蒸馏B.用浓硫酸脱水C.加入无水硫酸铜过滤D.加入新制的生石灰蒸馏5.一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2、H2O的总质量为13.8g,若其中水的质量为5.4g则二氧化碳的质量为()A.0.7gB.7.7gC.4.4gD.2.2g~4.4g之间6.近几年,我国连续发生了几起严重的假酒中毒事件,其原因主要是由于饮用酒中含有大量的()A、甲醇B、乙醇C、甲醛D、甲酸5第二课时乙酸【学习目标】1、认识乙酸的物理性质和用途2、通过实验探究,掌握乙酸的化学性质,包括酸性和酯化反应3、学会运用结构分析物质的性质【学习重点】乙酸的酯化反应【学习难点】从结构分析乙酸的酯化反应的机理【课前预习区】阅读教材p78-80,思考1、是食醋的主要成分,所以乙酸俗称。乙酸是一种有强烈气味的。当温度低于时,乙酸就凝结成像冰一样的晶体,所以无水乙酸又称。2、乙酸的分子结构分子式,结构式,结构简式3、乙酸的酸性①乙酸具有酸性,电离方程式为②乙酸遇石蕊试液变③与钠反应:;④与CaO反应:⑤与氢氧化钠溶液反应(离子方程式);⑥与碳酸钠溶液反应(离子方程式);该反应说明乙酸的酸性比碳酸。⑦乙酸钠与盐酸反应的方程式为:;该反应说明乙酸的酸性比盐酸。【课堂互动区】一、乙酸的分子结构与物理性质1、乙酸又称,分子式,结构式和结构简式分别是;2、乙酸的物理性质【实验探究1】(1)试根据乙酸的名称和结构推测其化学性质。(2)设计实验证明乙酸具有酸性。6可提供的实验药品有:乙酸溶液,锌片,碳酸钠溶液,氢氧化钠溶液,紫色石蕊试液,酚酞溶液。实验方案实验现象结论(化学方程式)实验1实验2实验3实验4【归纳总结】二、乙酸的化学性质1.乙酸的酸性(1)乙酸具有一元弱酸性,电离方程式为,(2)乙酸是一种常见的有机酸,酸性比碳酸弱,写出能证明乙酸酸性比碳酸酸性强的化学方程式。【迁移应用】烧开水的壶和盛放开水的暖瓶,使用一段时间后内壁会结上一层水垢,水垢的主要成分是CaCO3和Mg(OH)2。使用厨房中现有的物品如何除去水垢呢?写出有关的化学方程式。【实验探究2】在一支试管中加入3mL乙醇和2mL乙酸的混合物,然后边摇动试管边慢慢加入2mL浓硫酸,连接好后,小心加热,观察并记录实验现象。实验现象[问题组](1)浓硫酸的作用是什么?(2)饱和碳酸钠溶液的作用是什么?(3)加热的目的是什么?(4)导管的作用是什么?能不能将导管插到液面以下?为什么?【归纳总结】2.与乙醇的酯化反应(1)写出乙酸与乙醇反应方程式。(2)乙醇和乙酸反应原理是。若用含有18O的乙醇(即CH3CH218OH)与乙酸发生反应,18O将出现在哪些物质中?写出反应的化学方程式。(3)酯化反应是。7【拓展整理】根据乙酸的结构式,总结乙酸所能发生的化学反应。想一想,乙酸在发生反应时哪些化学建会发生断裂?请试着将你的想法填入下表乙酸发生反应的化学方程式反应类型断裂的价键【课堂巩固区】1.关于乙酸的下列说法中不正确的是()A.乙酸易溶于水和乙醇B.无水乙酸又称冰醋酸,它是纯净物C.乙酸是一种重要的有机酸,是有刺激性气味的液体D.乙酸分子里有四个氢原子,所以不是一元酸2.酯化反应属于()A.中和反应B.不可逆反应C.离子反应D.取代反应3.下列物质的溶液中,不易被氧化,不易被分解且能存放在玻璃试剂瓶中的是()A.氢氟酸B.次氯酸C.碳酸D.醋酸4.下列物质中最难电离出H+的是()A.CH3COOHB.C2H5OHC.H2OD.H2CO35.胆固醇是人体必需的生物活性物质,分子式为C25H46O,有一种胆固醇酯是液晶材料,分子式为C32H50O2,生成这种胆固醇酯的酸是()A.C6H13COOHB.C6H5COOHC.C7H15COOHD.C6H5CH2COOH6.巴豆酸的结构简式为CH3—CH=CH—COOH。现有①氯化氢、②溴水、③纯碱溶液、④丁醇、⑤酸性高锰酸钾溶液,判断在一定条件下,能与巴豆酸反应的物质是()A.仅②④⑤B.仅①③④C.仅①②③④D.全部8【课后巩固区】1.有绿色植物的废弃物(如秸秆、麦秸)为有机原料(已知:秸秆在一定条件下可以转化生成乙醇,乙醛可以被氧化成乙酸),选择必要的无机试剂合成下列物质(写出化学方程式并注明反应条件):(1).乙酸乙酯(2).乙二酸乙二酯2.(2003年高考化学单科卷)A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分数为8.82%;A只含有一种官能团,且每个碳原子上最多只连一个官能团:A能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。请填空:⑴A的分子式是,其结构简式是。⑵写出A与乙酸反应的化学方程式:。⑶写出所有满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。这些同分异构体的结构简式是。2.(1)具有支链的化合物A的分子式为C4H9O2,A可以使Br2的四氯化碳溶液褪色。1molA和1molNaHCO3能完全反应,则A的结构简式是。(2)化合物B含有C、H、O三种元素,分子量为60,其中碳的质量分数为60%,氢的质量分数为13.3%。B在催化剂Cu的作用下被氧气氧化成C,则B的结构简式是(3)D在NaOH水溶液中加热反应,可生成A的钠盐和B,相应反应的化学方程式是




 三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
本文标题:乙醇乙酸学案
链接地址:https://www.777doc.com/doc-2768940 .html