当前位置:首页 > 医学/心理学 > 药学 > 分子靶向药物在淋巴瘤中的应用
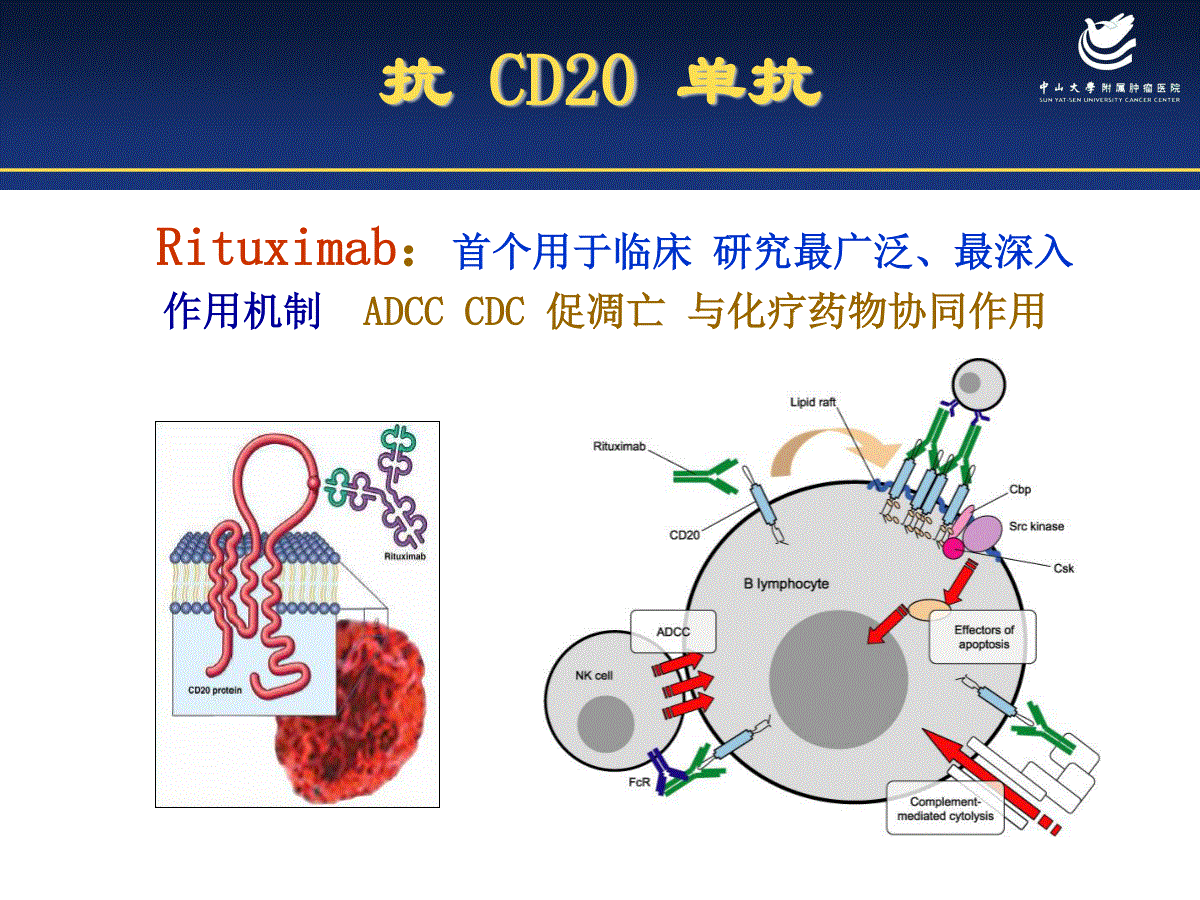
分子靶向治疗在淋巴瘤中的应用中山大学肿瘤医院淋巴瘤研究中心姜文奇治疗淋巴瘤的主要靶向药物单克隆抗体治疗抗CD20单抗抗CD22单抗抗CD52单抗抗CD30单抗放射免疫治疗I131-抗CD20抗体钇90-抗CD20抗体其他新型靶向药物组蛋白乙酰化酶抑制剂蛋白酶体抑制剂m-TOR抑制剂地尼白介素IL-2R维甲酸类抗血管生成治疗分子靶向药物的关键问题1234特异性,仅在肿瘤细胞中表达表达稳定均一、不产生分泌型抗原参与细胞凋亡/细胞生长信号的调节结合后不会出现明显的脱落靶抗原的选择抗CD20单抗Rituximab:首个用于临床研究最广泛、最深入作用机制ADCCCDC促凋亡与化疗药物协同作用淋巴瘤治疗新抗体靶向药物的不断涌现推动靶向治疗时代的到来惰性淋巴瘤分子靶向新药治疗进展滤泡性淋巴瘤治疗中存在的问题FL自然病程8~10年,III/IV期多见–晚期患者仍然无法治愈–复发/缓解交替–对治疗的缓解持续时间随着疾病进展而缩短–可发生转化100-80-60-40-20-0--------024681012时间(年)缓解率%1sttreatment3rd2nd4thGallagherC,etal.JClinOncol1986;4:1470–1480.患者(%)1987–19961976–19861960–1975年1008060402000510152025302000–2010利妥昔单抗改善滤泡性淋巴瘤患者的生存利妥昔单抗联合化疗治疗初治/复发难治性FL三个治疗方案长期随访结果研究方案随访时间中位TTFOSR-CVPvsCVP42月27月:6.6月(p0.0001)(预估3年)89%:81%(p=0.055)1R-CHOPvsCHOP18月未达到:29月(p0.0001)(预估2年)95%:90%(p=0.016)2R-MCPvsMCP37月54月:25月(PFS)(p0.0001)(3年)88%:74%(p=0.014)31.Solal-Celigny,etal.Blood2005;106:Abs.3502.HiddemannW,etal.Blood2005;106:Abs.3725-323.HiddemannW,etal.Blood2005;106:Abs.3725-321GhielminiM,etal.Blood2004;103:4416–232HochsterHS,etal.Blood2005;106:106a(Abstract349)3vanOersMHJ,etal.Blood2006研究组试验患者诱导治疗维持vs观察无病生存时间SAKK35/98PhaseIII初治/复发美罗华EFS↑1223月ECOG1496PhaseIII初治CVPPFS↑1561月EORTC20981PhaseIII复发CHOP±RPFS↑1552月利妥昔单抗维持治疗FL显示生存优势GhielminiM,etal.Blood2004;103:4416–23PD退出随机利妥昔单抗维持治疗组(375mg/m2每2月1次,共4次)滤泡性淋巴瘤(n=202)利妥昔单抗(375mg/m2/周x4)SDPRCR观察组评估(第12周)SAKK35/98研究:利妥昔单抗诱导治疗后利妥昔单抗维持治疗初治/复发FL方案SAKK35/98研究的最新结果:利妥昔单抗诱导治疗后利妥昔单抗维持治疗初治/复发FLGhielminiM,etal.ASCO2009.Abstract85123456780.10.20.30.40.50.60.70.80.91.0ProbabilityYrsSinceStartofTreatment00910中位随访时间:9.4年12ProlongedStandard25%inprolongedarmstillinremissionat8yrs(P=.0007)中位无事件生存时间延长11月P=0.0007人源化CD20单抗Veltuzumab治疗难治/复发性NHL的I/II期临床研究N=82(FL55例,其他27例)中位先前治疗疗程:2含美罗华治疗方案:1个方案49例,2个以上方案24例Veltuzumab耐受性良好,未见III-IV度毒性Veltuzumab对难治/复发FLORR44%,CR27%;对MZLORR83%,CR33%;对DLBCLPR43%Veltuzumab低剂量下也有一定疗效,值得进一步研究JClinOncol2009,27:3346-3353.苯达莫司丁-美罗华(B-R)vsCHOP-R苯达莫司汀-美罗华CHOP-美罗华滤泡性华氏巨球蛋白血症边缘区小淋巴细胞套细胞RStiLNHL1-2003苯达莫司汀90mg/m2d1,2+美罗华d1,每四周为一周期,最多进行6周期.CHOP-R,每三周为一周期,最多进行6周期.(RummeletalASH2009Abs#405)各亚型的无进展生存期(PFS)01224364860720.00.10.20.30.40.50.60.70.80.91.001224364860720.00.10.20.30.40.50.60.70.80.91.001224364860720.00.10.20.30.40.50.60.70.80.91.001224364860720.00.10.20.30.40.50.60.70.80.91.0滤泡p=0,0281套细胞p=0,0146边缘区p=0.6210华氏巨球蛋白血症B-RB-RB-RB-RCHOP-RCHOP-RCHOP-RCHOP-Rp=0.0024(RummeletalASH2009Abs#405)抗CD22单抗VC2C2C2C2C2C2NC60%-80%的B-NHL细胞表达CD22滤泡性淋巴瘤、套细胞淋巴瘤和边缘区B细胞性淋巴瘤高表达CD22Anti-CD22与CD22结合后迅速内在化Epratuzumab:人源性IgG1抗CD22单抗抗CD22单抗复发滤泡性淋巴瘤剂量组总有效率(CR+PR)中位TTP360mg/m243%23.7月480mg/m227%弥漫大B细胞淋巴瘤240mg/m233%8.1月360mg/m215%480mg/m220%EpratuzumabI/II期临床试验结果抗CD52单抗CD52表达于不同分化阶段的淋巴细胞,以及单核、巨噬和嗜酸性粒细胞表达CD52水平:T-PLL>B-CLL>正常B细胞Alemtuzumab(Campath-1H,阿仑单抗)为人源性IgG1型单抗抗CD52单抗抗瘤作用机制:ADCC及CDC作用FDA已批准Alemtuzumab作为氟达拉滨耐药的CLL的一线治疗,可单独使用Alemtuzumab单独用于CLL疗效优于瘤可宁等化疗药德国CLL2H研究德国慢性淋巴细胞性白血病研究组多中心前瞻性II期临床研究静脉用抗CD52单抗Alemtuzumab(Campath)对氟达拉滨耐药CLL患者ORR33%,中位OS16m;但注射相关副作用明显Alemtuzumab皮下注射可降低注射相关副作用,且药动学显示皮下注射血药浓度与静脉注射相当氟达拉滨对17p-和TP53突变CLL患者疗效不佳109例患者入组,103例接受Alemtuzumab治疗,第一阶段(46例)剂量爬升,第二阶段(57例)修订剂量JClinOncol2009,27:3994-4001ORR34%,CR4%,PR30%,SD38%,PD24%中位随访时间37.9个月,中位OS19.1个月,PFS7.7个月,TTTF5.6个月35例有效患者的中位缓解时间是13.7个月Alemtuzumab皮下注射与静脉注射等效且安全与化疗不同的是,Alemtuzumab可克服VH突变状态、TP53突变、17p-和11q-对CLL患者预后的不良影响JClinOncol2009,27:3994-4001放射免疫治疗用于淋巴瘤•I131-抗CD20抗体(Bexxar)用于治疗低度恶性淋巴瘤,ORR97%,CR63%(48/68),3年PFS68%,血液学毒性轻•Y90-抗CD20抗体(Zevalin)对侵袭性NHLORR67%,对低度恶性NHLORR82%。亦试用低度恶性淋巴瘤的维持治疗以及在自体造血干细胞移植中代替TBI.•与美罗华比较,主要不良反应为4度血小板减少(10%)和中性粒细胞减少(28%)。放射免疫治疗用于淋巴瘤蛋白酶体抑制剂蛋白酶体在细胞周期调控中起重要作用,因而成为抗肿瘤治疗的靶点之一Bortezomib(Velcade)是已上市的第一个蛋白酶体抑制剂临床前研究显示Velcade抑制多种B细胞性恶性肿瘤(如多发性骨髓瘤、弥漫大B细胞性NHL、套细胞性NHL、HD等)的蛋白酶体活性,促进细胞凋亡,增加肿瘤细胞对化疗和放疗的敏感性VERTICAL研究:VBR治疗复发/难治性FL背景:苯达莫司汀的剂量递增:50、70、90mg/m2/d;MTD未达到推荐与VR联合的苯达莫司汀剂量为90mg/m2主要终点:评价硼替佐米、苯达莫司汀和利妥昔单抗(VBR)治疗复发或难治性FL的CR率次要终点:ORR(CR+部分缓解[PR])、无进展生存时间(PFS)、以及缓解持续时间(DOR)评价VBR的安全性和耐受性Fowleretal.ASH2009;Abs933–datafromoralpresentation研究者评价的VBR最佳疗效最佳疗效末次既往治疗(N=63)VBR(N=59)ORR,n(%)37(59)51(86)CR20(32)31(53)PR17(27)20(34)SD,n(%)18(29)5(8)PD,n(%)7(11)3(5)与末次既往治疗相比较,VBR提高了缓解率以及缓解程度中位随诊时间为177天;11例(17%)患者仍在治疗中Fowleretal.ASH2009;Abs933–datafromoralpresentation不良事件n,(%)N=63所有AE63(100)3级AE44(70)药物相关性AE63(100)3级38(60)严重AE20(32)造成停药的AE12(19)治疗期间死亡1例(2%)8(13%)例患者因为疾病进展而退出研究VBR对于包括既往多次治疗过的患者(46%≥3种既往治疗)以及高危患者的患者是有效的但需注意患者耐受性的问题Fowleretal.ASH2009;Abs933–datafromoralpresentation硼替佐米联合CVP-R治疗初治FL患者方案:III/IVFL患者接受最多8个疗程的硼替佐米、环磷酰胺、长春新碱(最大2mg)、泼尼松和利妥昔单抗在医生慎重的判断过最终疗效之后,容许进行利妥昔单抗维持治疗终点:CR/CRu3-4级神经毒性的发生率结果:入选了95例患者,中位年龄56.6岁CVP-R的耐受性好:–无1例患者出现4级神经毒性,只有6例患者出现3级神经毒性–5例患者出现3-4级贫血;3例患者出现3-4级血小板减少Sehnetal.ASH2009;Abs407中期分析:CVP-R的疗效结论:CVP-R中加入硼替佐米是可行的,耐受性好和毒性小目前正在计划进行硼替佐米联合CVP-R的III期研究结果HRCR/Cru47%95%CI36.4%-58.5%PR37%—ORR84.6%76.6%-96.6%SD5/78—PD7/78—Sehnetal.ASH2009;Abs40778/95例患者可以评价治疗疗效,58.6%患者接受了利妥昔单抗的维持治疗弥漫大B细胞淋巴瘤分子靶向治疗进展弥漫大B细胞淋巴瘤治疗中存在问题Fisheretal.NEnglJMed.1993;328:1002.年患者死亡3年生存预测CHOP-212268854%m-BACOD2239352%ProMACE-CytaBOM2339750%MACOP-B2189350%1008060402000123456CHOPm-BACODProMACE-CytaBOMMACOP-B生存率(%)利妥昔单抗联合化疗改善DLBCL患者生存R-CHOPCHOPP值




 三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
本文标题:分子靶向药物在淋巴瘤中的应用
链接地址:https://www.777doc.com/doc-355517 .html