当前位置:首页 > 行业资料 > 能源与动力工程 > 化学平衡图像分析经典例题与习题附答案
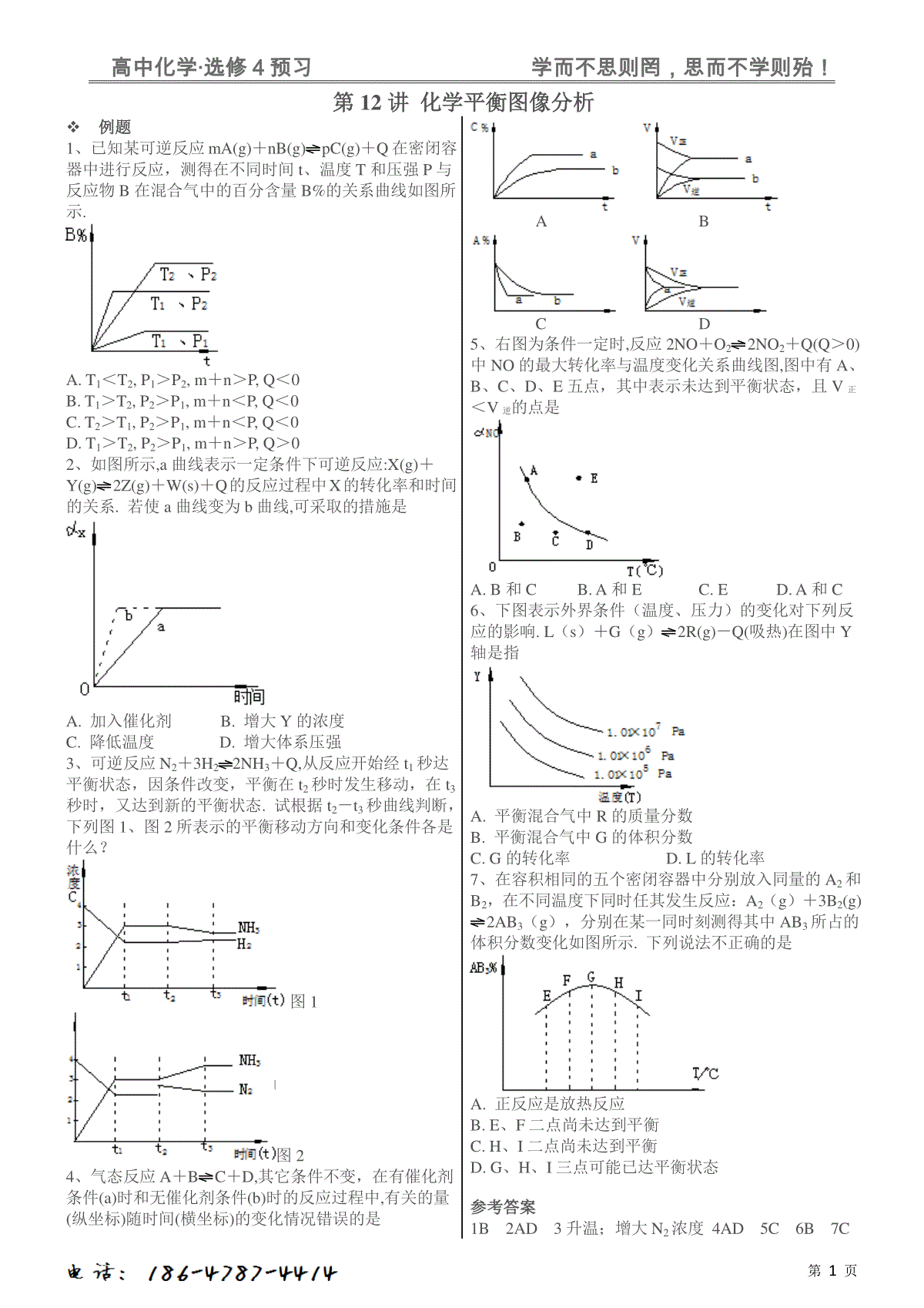
高中化学·选修4预习学而不思则罔,思而不学则殆!第1页第12讲化学平衡图像分析例题1、已知某可逆反应mA(g)+nB(g)pC(g)+Q在密闭容器中进行反应,测得在不同时间t、温度T和压强P与反应物B在混合气中的百分含量B%的关系曲线如图所示.A.T1<T2,P1>P2,m+n>P,Q<0B.T1>T2,P2>P1,m+n<P,Q<0C.T2>T1,P2>P1,m+n<P,Q<0D.T1>T2,P2>P1,m+n>P,Q>02、如图所示,a曲线表示一定条件下可逆反应:X(g)+Y(g)2Z(g)+W(s)+Q的反应过程中X的转化率和时间的关系.若使a曲线变为b曲线,可采取的措施是A.加入催化剂B.增大Y的浓度C.降低温度D.增大体系压强3、可逆反应N2+3H22NH3+Q,从反应开始经t1秒达平衡状态,因条件改变,平衡在t2秒时发生移动,在t3秒时,又达到新的平衡状态.试根据t2-t3秒曲线判断,下列图1、图2所表示的平衡移动方向和变化条件各是什么?图1图24、气态反应A+BC+D,其它条件不变,在有催化剂条件(a)时和无催化剂条件(b)时的反应过程中,有关的量(纵坐标)随时间(横坐标)的变化情况错误的是ABCD5、右图为条件一定时,反应2NO+O22NO2+Q(Q>0)中NO的最大转化率与温度变化关系曲线图,图中有A、B、C、D、E五点,其中表示未达到平衡状态,且V正<V逆的点是A.B和CB.A和EC.ED.A和C6、下图表示外界条件(温度、压力)的变化对下列反应的影响.L(s)+G(g)2R(g)-Q(吸热)在图中Y轴是指A.平衡混合气中R的质量分数B.平衡混合气中G的体积分数C.G的转化率D.L的转化率7、在容积相同的五个密闭容器中分别放入同量的A2和B2,在不同温度下同时任其发生反应:A2(g)+3B2(g)2AB3(g),分别在某一同时刻测得其中AB3所占的体积分数变化如图所示.下列说法不正确的是A.正反应是放热反应B.E、F二点尚未达到平衡C.H、I二点尚未达到平衡D.G、H、I三点可能已达平衡状态参考答案1B2AD3升温;增大N2浓度4AD5C6B7C高中化学·选修4预习学而不思则罔,思而不学则殆!第2页习题1、如右图所示表示平衡混合物中x的百分含量在不同的压强下,随温度变化的情况,在下列平衡体系中,x可以代表用下横线标明的物质(反应中各物质为气态)的是A.N2+2H22NH3△H<0B.H2+I22HI△H<0C.2SO32SO2+O2△H>0D.4NH3+5O24NO+6H2O△H<02、在溶积固定的4L密闭容顺中,进行可逆反应:X(气)+2Y(气)2Z(气)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率υ(正)、υ(逆)与时间t的关系如右图,如图中阴影部分面积表示A.X的浓度的减少B.Y的物质的量的减少C.Z的浓度的增加D.X的物质的量的减少3、今有反应X(g)+Y(g)2Z(g)+△H<0若反应开始经t1秒后达到平衡,又经t2秒后,由于反应条件的改变使平衡破坏,则t3时又达到平衡,如图表示,试分析,以t2到t3秒曲线变化的原因是A.增大了X和Y的浓度B.使用了催化剂C.增加了反就体系的压强D.升高了反应的温度4、对达到平衡状态的可逆反应X+YZ+W,在其他条件不变的情况下,增大压强,反应速率变化图象如右图所示,则图象中关于X、Y、Z、W四种物质的聚集状态为A.Z、W均为气体,X、Y中有一种是气体B.Z、W中有一种是气体,X、Y皆非气体C.X、Y、Z、W皆非气体D.X、Y均为气体,Z、W中有一种为气体5、已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是A.该反应在T1、T3温度时达到过化学平衡B.该反应在T2温度时达到过化学平衡C.该反应的逆反应是放热反应D.升高温度,平衡会向正反应方向移动6、右图表示反应N2(g)+3H2(g)2NH3(g);ΔH=-92.2kJ/mol。在某段时间t0~t6中反应速率与反应过程的曲线图,则氨的百分含量最高的一段时间是A.t0~t1B.t2~t3C.t3~t4D.t5~t67、在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应,平衡后测得X,Y的转化率与起始时两物质的物质的量之比nx/ny的关系如图所示,则X,Y的反应方程式可表示为A.2X+Y3ZB.3X+2Y2ZC.X+3YZD.3X+YZ8、对于可逆反应:A2(g)+3B2(g)2AB3(g)(正反应放热),下列图象中正确的是ABCD参考答案1D2C3D4A5B6A7D8AB

 三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
本文标题:化学平衡图像分析经典例题与习题附答案
链接地址:https://www.777doc.com/doc-5559881 .html