当前位置:首页 > 商业/管理/HR > 质量控制/管理 > 高优指导高三化学一轮复习-滚动测试卷一(第一二单元)新人教版
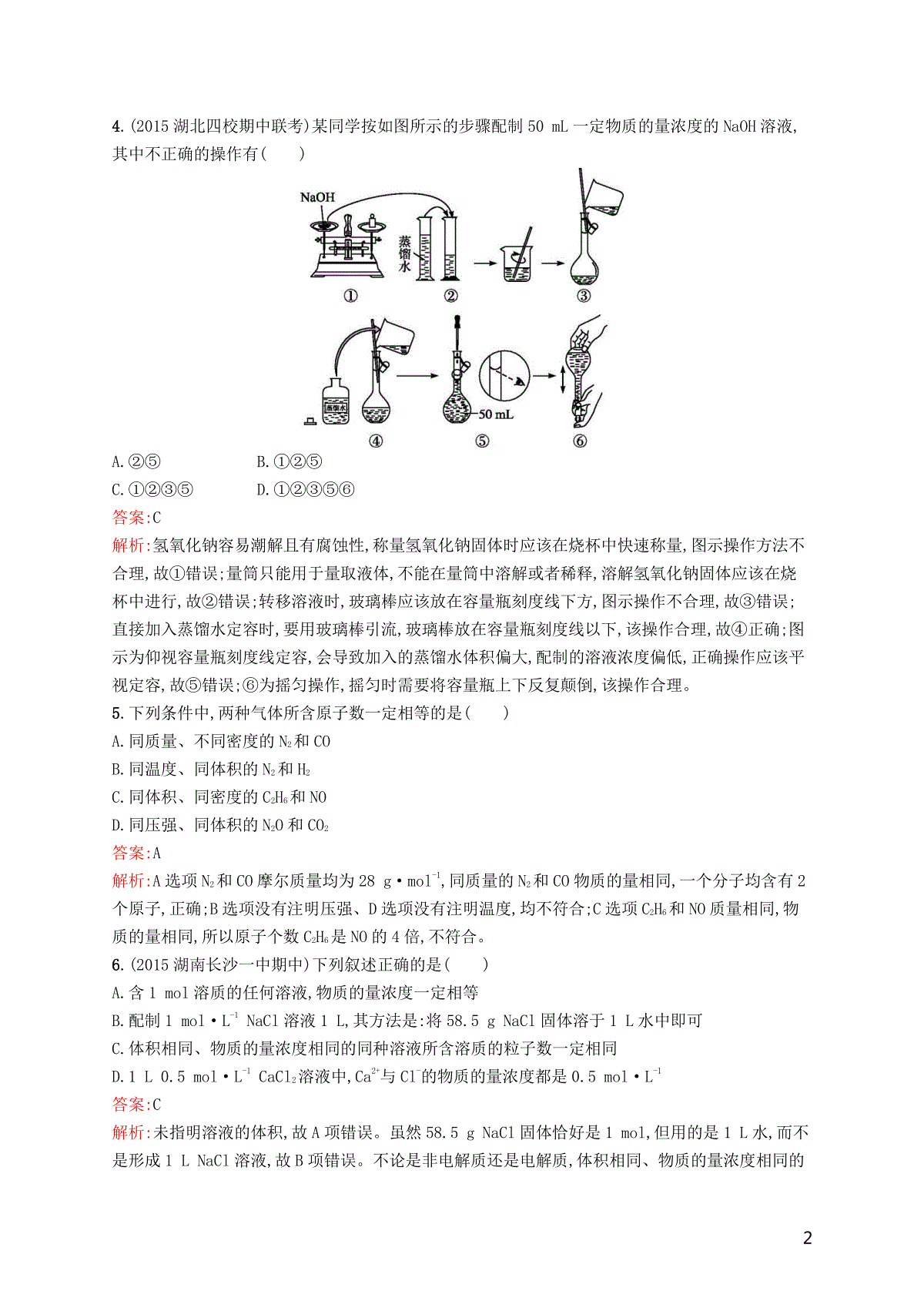
1滚动测试卷一(第一~二单元)(时间:90分钟满分:100分)一、选择题(本题共18小题,每小题3分,共54分,每小题只有一个选项符合题目要求)1.(2015河北石家庄五校联考)下列现象不是因为发生化学变化而产生的是()A.皮肤不慎沾上浓硝酸而呈黄色B.久置的KI溶液呈黄色C.盛在无色试剂瓶中的浓硝酸呈黄色D.食盐撒在燃着的液化气的火焰上,火焰呈黄色答案:D解析:皮肤中的蛋白质遇浓硝酸发生蛋白质的颜色反应而呈黄色,故A不符合题意;久置的KI溶液呈黄色是因为溶液中的I-被空气中的氧气氧化生成碘单质,故B不符合题意;浓硝酸呈黄色是由于浓硝酸分解产生的NO2溶于溶液中所致,故C不符合题意;火焰呈现黄色只是钠元素的焰色反应,并非有新物质生成,不属于化学变化,故D符合题意。2.(2015江西九校联考)下列有关物质分类或归类正确的一组是()①酸性氧化物:SO2、NO、CO2、SiO2②氢氟酸、盐酸、水玻璃、氨水均为混合物③明矾、小苏打、硫酸钡、HClO均为电解质④碘酒、牛奶、豆浆、漂粉精均为胶体⑤液氨、液氯、干冰、碘化银均为化合物A.①和③B.②和③C.③和④D.②和⑤答案:B解析:①SO2、CO2、SiO2为酸性氧化物,NO为不成盐氧化物,错误;②氢氟酸、盐酸、水玻璃、氨水均为混合物,正确;③明矾、小苏打、硫酸钡、HClO均为电解质,正确;④碘酒为碘的酒精溶液,牛奶、豆浆属于胶体,漂粉精为固体混合物,错误;⑤液氨、干冰、碘化银为化合物,液氯为单质,错误。3.某学习兴趣小组讨论辨析以下说法:①通过化学变化可以实现16O与18O间的相互转化;②灼烧钠的化合物时,火焰呈黄色,发生化学反应;③碱性氧化物一定是金属氧化物;④只由一种元素组成的物质一定为纯净物;⑤石墨和C60具有相似的化学性质;⑥糖类、蛋白质、油脂属于天然高分子化合物,其中说法正确的是()A.①②B.③⑤C.①③④D.③⑤⑥答案:B解析:①16O与18O互为同位素,它们之间的转化不属于化学变化,错误;②焰色反应过程中没有新物质生成,不发生化学变化,错误;③碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物,正确;④只由一种元素组成的物质不一定为纯净物,如氧气与臭氧组成的物质属于混合物,错误;⑤石墨和C60都是由C原子构成的,所以具有相似的化学性质,正确;⑥蛋白质属于天然高分子化合物,而糖类不都属于高分子化合物,如葡萄糖是单糖,油脂不属于高分子化合物,错误。24.(2015湖北四校期中联考)某同学按如图所示的步骤配制50mL一定物质的量浓度的NaOH溶液,其中不正确的操作有()A.②⑤B.①②⑤C.①②③⑤D.①②③⑤⑥答案:C解析:氢氧化钠容易潮解且有腐蚀性,称量氢氧化钠固体时应该在烧杯中快速称量,图示操作方法不合理,故①错误;量筒只能用于量取液体,不能在量筒中溶解或者稀释,溶解氢氧化钠固体应该在烧杯中进行,故②错误;转移溶液时,玻璃棒应该放在容量瓶刻度线下方,图示操作不合理,故③错误;直接加入蒸馏水定容时,要用玻璃棒引流,玻璃棒放在容量瓶刻度线以下,该操作合理,故④正确;图示为仰视容量瓶刻度线定容,会导致加入的蒸馏水体积偏大,配制的溶液浓度偏低,正确操作应该平视定容,故⑤错误;⑥为摇匀操作,摇匀时需要将容量瓶上下反复颠倒,该操作合理。5.下列条件中,两种气体所含原子数一定相等的是()A.同质量、不同密度的N2和COB.同温度、同体积的N2和H2C.同体积、同密度的C2H6和NOD.同压强、同体积的N2O和CO2答案:A解析:A选项N2和CO摩尔质量均为28g·mol-1,同质量的N2和CO物质的量相同,一个分子均含有2个原子,正确;B选项没有注明压强、D选项没有注明温度,均不符合;C选项C2H6和NO质量相同,物质的量相同,所以原子个数C2H6是NO的4倍,不符合。6.(2015湖南长沙一中期中)下列叙述正确的是()A.含1mol溶质的任何溶液,物质的量浓度一定相等B.配制1mol·L-1NaCl溶液1L,其方法是:将58.5gNaCl固体溶于1L水中即可C.体积相同、物质的量浓度相同的同种溶液所含溶质的粒子数一定相同D.1L0.5mol·L-1CaCl2溶液中,Ca2+与Cl-的物质的量浓度都是0.5mol·L-1答案:C解析:未指明溶液的体积,故A项错误。虽然58.5gNaCl固体恰好是1mol,但用的是1L水,而不是形成1LNaCl溶液,故B项错误。不论是非电解质还是电解质,体积相同、物质的量浓度相同的3同种溶液所含溶质的粒子数必然相同,故C项正确。CaCl2是强电解质,溶于水能完全电离成Ca2+和Cl-,在1L0.5mol·L-1CaCl2溶液中,Ca2+和Cl-的物质的量浓度分别是0.5mol·L-1和1.0mol·L-1,故D项错误。7.硫酸铝、硫酸钾、明矾三种物质组成的混合物中,当S的浓度为0.20mol·L-1时,加入等体积的0.20mol·L-1KOH溶液(混合后溶液体积变化忽略不计),使生成的白色沉淀恰好溶解,那么最后混合物中K+的物质的量浓度是()A.0.20mol·L-1B.0.25mol·L-1C.0.225mol·L-1D.0.45mol·L-1答案:C解析:根据电荷守恒,原溶液中c(K+)+3c(Al3+)=2c(S),c(S)=0.20mol·L-1,加入等体积的0.20mol·L-1KOH溶液,恰好使Al3+生成的Al(OH)3沉淀溶解,由Al3+~4OH-知,原溶液中c(Al3+)=0.05mol·L-1,代入公式c(K+)+3×0.05mol·L-1=2×0.20mol·L-1,解得:c(K+)=0.25mol·L-1。设三种物质的混合溶液的体积为VL,则混合溶液中n(K+)=0.25Vmol,后加的等体积的KOH溶液中n(K+)=0.20Vmol,故混合后c(K+)=mol·L-1=0.225mol·L-1,C项正确。8.(2015福建漳州质检)ClO2是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO42ClO2↑+K2SO4+2CO2↑+2H2O。据此,下列说法不正确的是()A.KClO3发生还原反应B.H2C2O4在反应中被氧化C.H2C2O4的氧化性强于ClO2的氧化性D.每生成1molClO2,转移的电子数约为6.02×1023答案:C解析:题给反应中KClO3是氧化剂,发生还原反应,H2C2O4是还原剂,在反应中被氧化,每生成1molClO2,转移电子的物质的量为1mol,所以A、B、D都正确;在氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,还原剂的还原性强于还原产物的还原性,所以H2C2O4的还原性强于ClO2的还原性,C不正确。9.(2015四川成都模拟)能正确表示下列反应的离子方程式是()A.金属铝溶于稀硫酸中:Al+2H+Al3++H2↑B.KI溶液中滴入稀硫酸,空气中振荡:4H++4I-+O22I2+2H2OC.CuCl2溶液中加入氨水:Cu2++2OH-Cu(OH)2↓D.向NH4HCO3溶液中加过量的NaOH溶液并加热:N+OH-NH3↑+H2O〚导学号25730488〛答案:B解析:A选项,离子方程式未配平,错误;C选项,一水合氨不能拆,错误;D选项,HC先与OH-反应,错误。10.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲乙丙。4下列有关物质的推断不正确的是()A.若甲为焦炭,则丁可能是O2B.若甲为SO2,则丁可能是氨水C.若甲为Fe,则丁可能是盐酸D.若甲为NaOH溶液,则丁可能是CO2答案:C解析:若甲为Fe,丁为盐酸,Fe与盐酸反应可生成FeCl2,但FeCl2不能与盐酸发生反应,因此C项错误。11.(2015山东19所名校第二次调研考试)在下列溶液中,各组离子一定能够大量共存的是()A.由水电离的c(H+)=1×10-4mol·L-1的溶液中:Ca2+、K+、Cl-、HCB.在pH=1的无色溶液中:Fe2+、Mg2+、N、Cl-C.含有大量Al3+的溶液中:Na+、Cl-、N、OH-D.含有大量OH-的溶液中:C、Cl-、F-、K+答案:D解析:由水电离的c(H+)=1×10-4mol·L-1的溶液中溶液呈酸性或者呈碱性,HC不能大量共存,A错误;在pH=1的无色溶液中Fe2+与N发生氧化还原反应,不能共存,B错误;Al3+与OH-不能大量共存,C错误;含有大量OH-的溶液中:C、Cl-、F-、K+能大量共存,D正确。12.(2015湖北七市(州)教科研协作体联考)下列化学反应先后顺序判断正确的是()A.在含有等物质的量的H+、Al3+的溶液中,逐滴加入NaOH溶液:H+、Al3+、Al(OH)3B.在含有等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+C.在含有等物质的量的NaCl、Na2S的溶液中加入AgNO3溶液:NaCl、Na2SD.在含有等物质的量的Fe3+、Cu2+的溶液中加入铁粉:Cu2+、Fe3+答案:A解析:酸性由强到弱为H+、Al3+、Al(OH)3,则逐滴加入NaOH溶液,反应先后顺序为H+、Al3+、Al(OH)3,故A正确;还原性由强到弱为I-、Fe2+、Br-,则缓慢通入氯气反应的先后顺序为I-、Fe2+、Br-,故B错误;溶度积大小顺序为Ksp(AgCl)Ksp(Ag2S),则加入AgNO3溶液反应的先后顺序为Na2S、NaCl,故C错误;氧化性为Fe3+Cu2+,则加入铁粉反应的先后顺序为Fe3+、Cu2+,故D错误。13.铬是人体必需的微量元素,它与脂类代谢有密切联系,能增强人体内胆固醇的分解和排泄,但铬过量会引起污染,危害人类健康。不同价态的铬的毒性不同,三价铬对人体几乎无毒,六价铬的毒性约为三价铬的100倍。下列叙述错误的是()A.发生铬中毒时,可服用维生素C缓解毒性,因为维生素C具有还原性B.K2Cr2O7可以氧化乙醇,该反应可用于检查酒后驾驶C.在反应Cr2+I-+H+Cr3++I2+H2O中,氧化产物与还原产物的物质的量之比为3∶2D.污水中的Cr3+在溶解的氧气作用下可被氧化为Cr2答案:D解析:维生素C具有还原性,可与六价铬反应生成无毒的三价铬,A正确;K2Cr2O7可将乙醇氧化为乙酸,同时反应后含铬化合物的颜色发生变化,B正确;反应Cr2+I-+H+Cr3++I2+H2O中,氧化产物为I2,5还原产物为Cr3+,根据得失电子守恒可知,二者的物质的量之比为3∶2,C正确;Cr2的氧化性比氧气的氧化性强,氧气不能将Cr3+氧化为Cr2,D错误。14.下列实验操作、现象和结论均正确的是()选项实验操作现象结论ASO2通入溴水中溶液褪色SO2有漂白性B将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液溶液变红Fe(NO3)2样品已氧化变质C将新制氯水和KI溶液在试管中混合后,加入CCl4,振荡、静置溶液分层,下层呈紫色氧化性:Cl2I2D分别向0.1mol·L-1醋酸和饱和硼酸溶液中滴加0.1mol·L-1Na2CO3溶液醋酸中有气泡产生,硼酸中没有气泡产生酸性:醋酸碳酸硼酸答案:D解析:SO2具有还原性,能使溴水褪色,A错误;在酸性溶液中硝酸根离子能氧化亚铁离子,生成铁离子,因此不能据此说明硝酸亚铁样品已经变质,B错误;溶液分层,下层呈紫色,说明反应中有碘生成,因此氧化性:Cl2I2,C错误;根据较强酸制备较弱酸可知,醋酸中有气泡产生,说明醋酸的酸性强于碳酸,硼酸中没有气泡产生,说明硼酸的酸性弱于碳酸,D正确。15.(2015河北保定期末调研)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性,已知:4Fe+10H2O4Fe(OH)3+8OH-+3O2↑。高铁酸钾常见制备方法之一是湿法制备:在一定条件下,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液。下列说法正确的是()A.K2FeO4在处理水的过程中所起的作用只有消毒杀菌B.同浓度的高铁酸钾在pH=11.50




 三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
本文标题:高优指导高三化学一轮复习-滚动测试卷一(第一二单元)新人教版
链接地址:https://www.777doc.com/doc-6914270 .html