当前位置:首页 > 行业资料 > 其它行业文档 > 高中化学 第三章 第三节用途广泛的金属材料课件 新人教版必修1
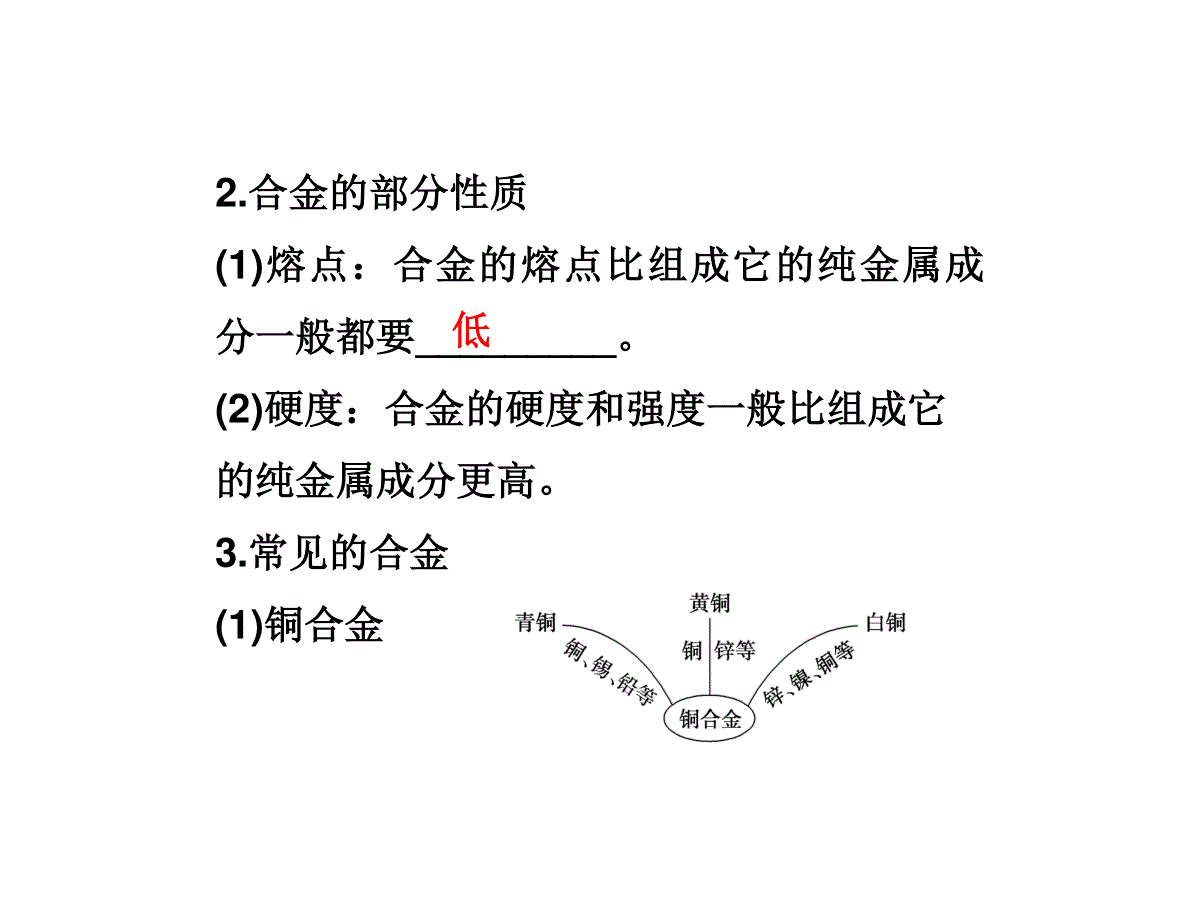
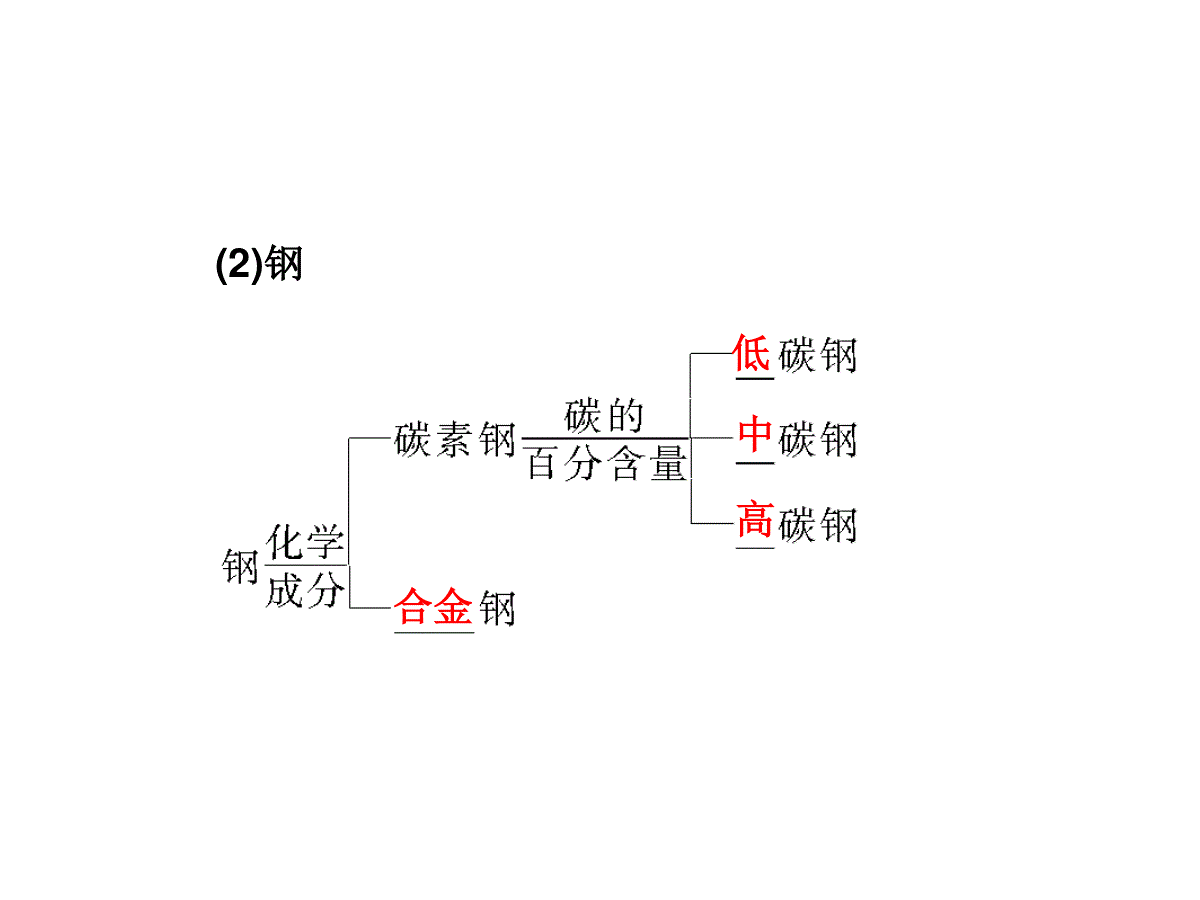
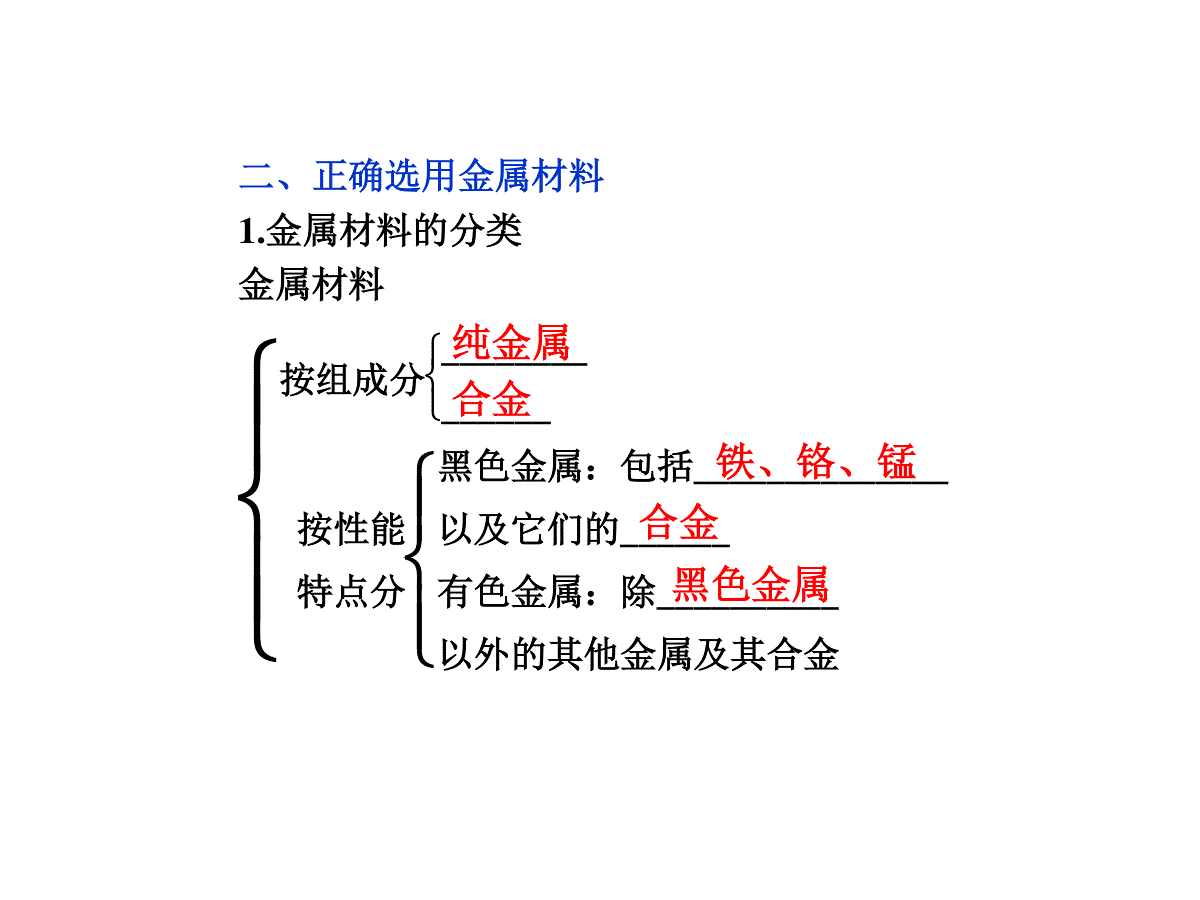
第三节用途广泛的金属材料第三章金属及其化合物新知初探自学导引自主学习一、常见合金的重要应用1.合金的定义合金是指由两种或两种以上的_________(或_______________)熔合而成的具有________特性的物质。金属金属与非金属金属2.合金的部分性质(1)熔点:合金的熔点比组成它的纯金属成分一般都要_________。(2)硬度:合金的硬度和强度一般比组成它的纯金属成分更高。3.常见的合金(1)铜合金低(2)钢低中高合金二、正确选用金属材料1.金属材料的分类金属材料按组成分______________按性能特点分黑色金属:包括______________以及它们的______有色金属:除__________以外的其他金属及其合金黑色金属纯金属合金铁、铬、锰合金2.金属材料的正确选用在进行金属材料的选择时,常常要考虑以下几个方面:主要用途、外观、物理性质、化学性质、价格、加工难度、日常维护、对环境的影响等方面。自主体验1.下列关于合金的叙述正确的是()①具有金属的特性②通过熔合而成③含有两种或两种以上金属或金属和非金属④一般来说,合金的熔点比各组分的熔点低A.仅①②B.仅③④C.仅②③④D.全部解析:选D。合金是由两种或两种以上的金属(或金属和非金属)熔合而成的具有金属特性的物质,其熔点一般低于成分金属,硬度高于成分金属。2.(2012·湖南长沙一中高一检测)下列所用材料不.属于合金的是()A.家用的铝窗B.建筑用的钢筋C.铸造用的黄铜D.温度计用的水银解析:选D.温度计用的水银是纯净物,不是合金.3.镁铝合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等,下列与这些用途无关的性质是()A.不易生锈B.导电性好C.密度小D.强度高解析:选B.建筑装潢材料不考虑其导电性好坏.要点突破讲练互动探究导引1镁铝合金为什么广泛应用于飞机?提示:因为镁铝合金的密度小,强度大。常见合金的成分及其重要用途探究导引2钛被称为“21世纪金属”,其合金大规模应用于航天航空,利用的是合金的哪些优点?提示:钛的合金具有密度小、强度高、耐腐蚀、耐高温等优点。要点归纳1.铜合金合金主要成分主要性能主要用途青铜铜、锡强度高、可塑性好、耐磨、耐腐蚀机械零件,如轴承、齿轮等合金主要成分主要性能主要用途黄铜铜、锌强度高、可塑性好、易加工、耐腐蚀机械零件、仪表、日用品白铜铜、镍光泽好、耐磨、耐腐蚀、易加工钱币、代替银做饰品2.合金钢名称主要合金元素主要特性主要用途锰钢锰韧性好,硬度大钢轨、轴承、钢模、挖掘机铲斗、坦克装甲名称主要合金元素主要特性主要用途不锈钢铬、镍抗腐蚀性好医疗器械、容器、反应釜、炊具硅钢硅导磁性好变压器、发电机和电动机中的铁芯钨钢钨耐高温、硬度大刀具3.铝合金4.钛合金钛的合金具有密度小、强度高、耐腐蚀、耐高温等优点,主要用于飞机、火箭、导弹、人造卫星、宇宙飞船等领域。成分元素主要特性主要用途Al、Mg、Cu、Si等密度小,强度大用于汽车、飞机、火箭、船舶制造特别提醒(1)合金的种类和性能与成分有关。不同的原料,不同的原料配比,不同的制造工艺,得到不同性能的合金。(2)由于合金的形成改变了金属的内部结构,所以对金属的物理性质和化学性质都有影响.如不锈钢的抗腐蚀性比纯铁强得多。即时应用(2012·东莞高一检测)合金与纯金属制成的金属材料相比,优点是()①合金的硬度一般比它的各成分金属的大;②一般地,合金的熔点比它的各成分金属的低;③改变原料的配比、改变生成合金的条件,可以得到具有不同性能的合金;④合金比纯金属的导电性能更强;⑤合金比纯金属的应用范围更广泛。A.①②③⑤B.②③④C.①②④D.①②④⑤解析:选A。合金一般比成分金属熔点低,硬度大,具有更好的机械加工性能,故应用范围更广泛,但合金的导电性却不一定比纯金属更强,比如铝合金的导电性比纯铝要差.题型探究权威预测合金的概念和性质例1根据下列金属的熔、沸点:金属NaCuAlFe熔点/℃97.510836601535沸点/℃883259522003000其中不.能形成合金的是(双选)()A.Cu与NaB.Fe与CuC.Fe与NaD.Al与Na【解析】合金是金属在熔化状态时相互溶解或相互混合形成的,熔化时的温度需达到两种金属中最高的金属的熔点,但又不能超出成分金属中的最低沸点的温度,选项中的Cu与Na、Fe与Na不符合合金要求。【答案】AC【易误警示】能形成合金的两种或两种以上的金属或金属与非金属必须熔点相近,否则不能熔合成合金。有关合金的计算例2某合金粉末11g,加入到足量的稀硫酸中,在标准状况下产生的气体体积为11.2L,此合金可能是()A.Mg、Al合金B.Cu、Zn合金C.Zn、Fe合金D.Mg、Zn合金【解析】设混合物的平均摩尔质量为M,化合价为+2,则:M+2H+=====M2++H2↑122.411M11.2M=22g·mol-1则+2价金属的摩尔质量:Mg—24、Al—18(23×27)、Zn—65、Fe—56、Cu不反应其摩尔质量比M大,只有假设的+2价Al的摩尔质量小于22,故选A。【答案】A【规律方法】解决此类习题规律性较强。一般方法是:设出该混合物的平均摩尔质量及对应的化合价,通过化学方程式,利用其他已知量求出在此化合价下的平均摩尔质量,平均摩尔质量在两物质(多种物质)摩尔质量之间即为答案。但要注意两点:(1)不与所给物质反应的物质的摩尔质量看作大于平均摩尔质量;(2)根据化合价换算对应的摩尔质量,如+1价Na换成+2价时,摩尔质量为23g·mol-1×2=46g·mol-1。热点示例思维拓展[经典案例]某学生想测定CuZn合金及Cu-Ag合金中铜的质量分数,实验室只提供了一瓶未标明浓度的稀盐酸和必要的仪器。请回答下列问题:(1)你认为在现有条件下能测出铜的质量分数的是哪种合金?(2)若该同学取该合金的粉末32.5g,与足量该盐酸充分反应,经测定产生了0.4g氢气,你能计算出该合金中铜的质量分数吗?【答案】(1)要用盐酸来测定铜合金中铜的质量分数,可以测得的是CuZn合金。因为在Cu、Zn、Ag三种金属中,只有锌跟盐酸反应放出氢气:Zn十2HCl===ZnCl2+H2↑.(2)设32.5gCuZn合金中含锌的质量为xZn+2HCl=====ZnCl2+H2↑65g2gx0.4g65gx=2g0.4gx=65g×0.4g2g=13g该合金中铜的质量分数为:32.5g-13g32.5g×100%=60%。


 三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
本文标题:高中化学 第三章 第三节用途广泛的金属材料课件 新人教版必修1
链接地址:https://www.777doc.com/doc-5978718 .html