当前位置:首页 > 商业/管理/HR > 质量控制/管理 > 物质的检验、分离和提纯课件
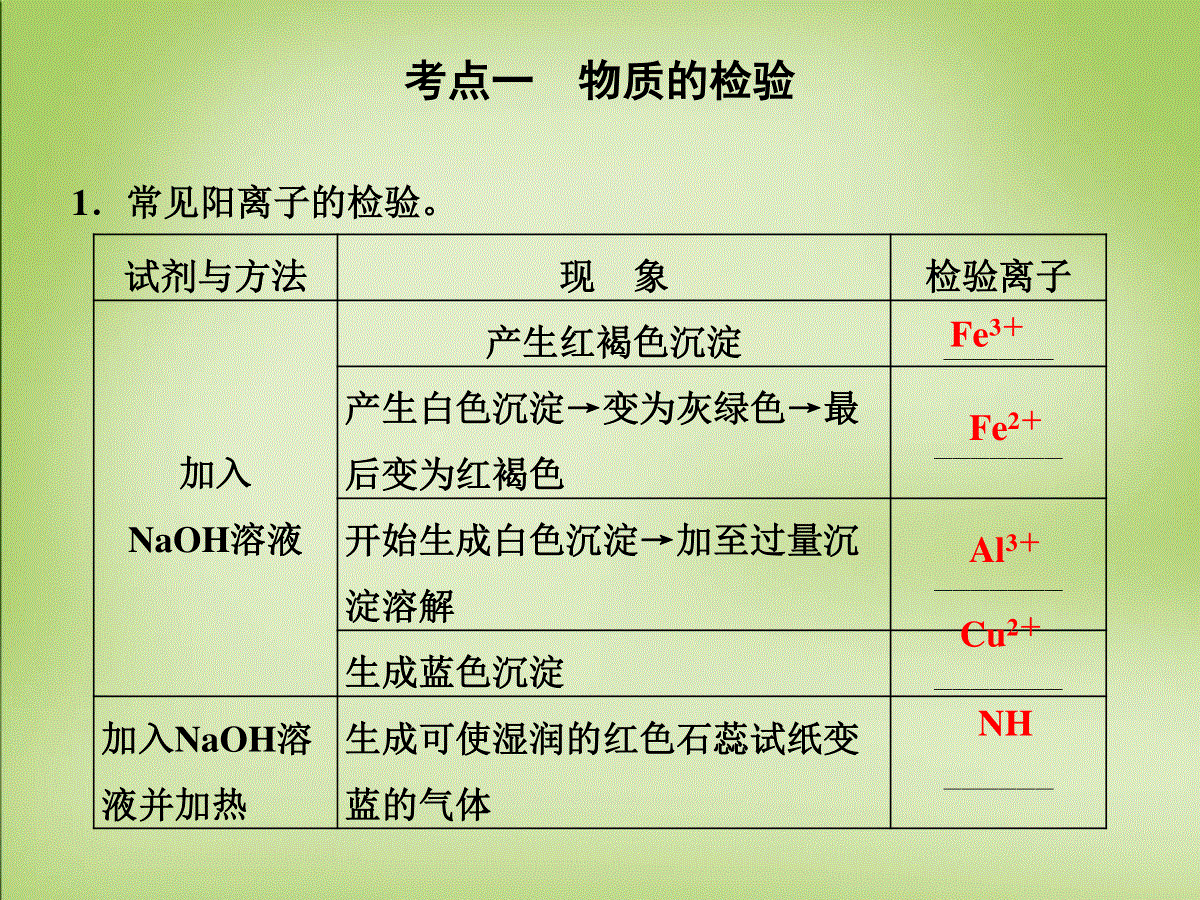
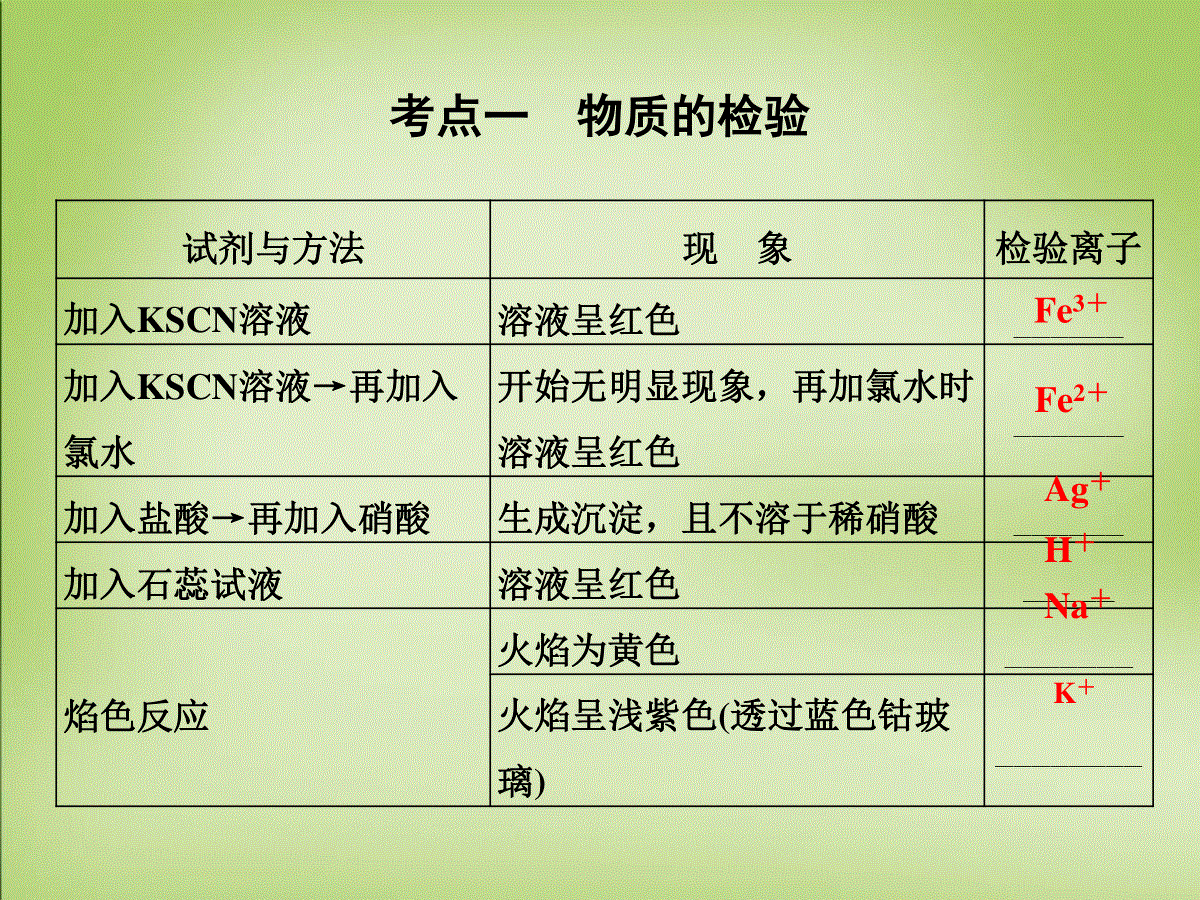
物质的检验、分离和提纯考纲要求1.能对常见物质进行检验。2.能对常见物质进行分离和提纯。考点一物质的检验1.常见阳离子的检验。试剂与方法现象检验离子加入NaOH溶液产生红褐色沉淀______产生白色沉淀→变为灰绿色→最后变为红褐色_______开始生成白色沉淀→加至过量沉淀溶解_______生成蓝色沉淀_______加入NaOH溶液并加热生成可使湿润的红色石蕊试纸变蓝的气体______Fe3+Fe2+Al3+Cu2+NH考点一物质的检验试剂与方法现象检验离子加入KSCN溶液溶液呈红色______加入KSCN溶液→再加入氯水开始无明显现象,再加氯水时溶液呈红色______加入盐酸→再加入硝酸生成沉淀,且不溶于稀硝酸______加入石蕊试液溶液呈红色_____焰色反应火焰为黄色_______火焰呈浅紫色(透过蓝色钴玻璃)________Fe3+Fe2+Ag+H+Na+K+考点一物质的检验2.常见阴离子的检验。试剂与方法现象检验离子加入硝酸银溶液和稀硝酸产生白色沉淀,且不溶于稀硝酸_____产生浅黄色沉淀,且不溶于稀硝酸______产生黄色沉淀,且不溶于稀硝酸_____先用盐酸酸化,无沉淀、气体生成,再加BaCl2溶液产生白色沉淀_____Cl-Br-I-SO42-考点一物质的检验试剂与方法现象检验离子先加氯化钡溶液,再加稀盐酸,生成的气体通入品红溶液先沉淀、后溶解,品红溶液褪色____32-先加氯化钡溶液,再加稀盐酸,生成的无色无味气体分别通入澄清石灰水先沉淀,后溶解,澄清石灰水变浑浊CO32-澄清石灰水不沉淀,澄清石灰水变浑浊_______加入氯水和四氯化碳,充分振荡溶液分层,下层为紫红色_____加入石蕊试液溶液变蓝色______加入酚酞试液溶液变红色SOHCO3-I-OH-考点一物质的检验4.常见气体的检验:(1)可燃性气体的检验。考点一物质的检验(2)酸性气体的检验。(3)碱性气体的检验(NH3)。(4)强氧化性气体的检验。考点一物质的检验考点一物质的检验(1)能使品红溶液褪色的气体有:SO2、Cl2、O3、NO2等,其中SO2只能使石蕊试液变红,而不能褪色,Cl2、O3、NO2最终可使石蕊试液褪色。(2)在中学化学中,氨气是唯一能使湿润的红色石蕊试纸变蓝的气体。(3)不溶于水也不溶于酸的盐的酸根一般是强酸根,如AgCl、BaSO4等。考点一物质的检验某补铁剂说明书如下:怎样用化学实验的方法检验有亚铁离子存在?取少量富马酸亚铁颗粒溶于水,向溶液中滴加________,溶液_________________,再滴入________,溶液变为________,说明在补铁剂中含有亚铁离子。富马酸亚铁颗粒,化学式:C4H2FeO4,每包含富马酸亚铁0.2g,适应症:缺铁性贫血,服用量:每次1~2包(成人)提示:KSCN溶液没有明显颜色变化氯水或H2O2红色题组一固、液物质的检验1.(2015·丰台模拟)为了证明(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)的成分中含有NH+4、Fe2+、SO2-4和H2O,取少量硫酸亚铁铵晶体放入试管,下列实验叙述中错误的是()A.加热,试管口有液体生成,则可证明晶体的成分中含有结晶水B.加少量水,溶液为浅绿色,滴入2滴KSCN溶液,溶液不显红色,再滴加几滴新制氯水,溶液变为红色,则证明晶体的成分中含有Fe2+DC.加水溶解,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO2-4D.加浓NaOH溶液,加热,用湿润的蓝色石蕊试纸放在试管口检验,试纸变红色,则证明晶体的成分中含有NH+42.某同学为检验溶液中是否含有常见的几种无机离子,进行了如图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是()题组一固、液物质的检验A.原溶液中一定含有SO2-4B.原溶液中一定含有NH+4C.原溶液中一定含有Cl-D.原溶液中一定含有Fe3+B原溶液中加入硝酸钡和盐酸生成白色沉淀,原溶液中可能存在SO2-4、SO2-3或Ag+,A错误;加硝酸银溶液产生白色沉淀,可能是加入的盐酸引起的,C错误;因检验过程中产生的气体能使湿润的红色石蕊试纸变蓝,说明原溶液中一定含有NH+4,B正确;加入KSCN溶液得到红色溶液,Fe3+可能是由原溶液中的Fe2+被H+、NO-3氧化而来的,故原溶液中不一定含有Fe3+,D错误。3.某溶液含有Ⅲ中的离子(见下表),欲用Ⅰ中的试剂来检验溶液是否还含有Ⅱ中的离子,能够成功检验的是(说明:在实验过程中不允许加热、过滤、萃取等操作)()选项ⅠⅡⅢA稀氨水Al3+Mg2+B稀硝酸、AgNO3溶液Cl-I-CKSCN溶液Fe2+Fe3+D稀盐酸、BaCl2溶液SOSODA项,稀氨水和Mg2+、Al3+反应都生成白色沉淀;B项,AgI沉淀的黄色将AgCl沉淀的白色掩盖;C项,Fe3+遇KSCN溶液呈红色;D项,SO2-3在稀盐酸中与Ba2+溶液不能生成BaSO3沉淀,而SO2-4与Ba2+在稀盐酸中反应生成白色沉淀BaSO4。题组一固、液物质的检验4.根据下列实验事实得出的结论正确的是()A.气体――――――――→通入品红溶液品红溶液褪色;结论:原气体一定是SO2B.气体――→点燃气体――――――――――→通入Ba(OH)2溶液白色沉淀;结论:原气体一定是烃C.某溶液――――――→打开瓶盖冒白雾――――――――→用蘸有浓氨水的玻璃棒靠近白烟;结论:原溶液一定是浓盐酸D.某有色溶液――――――――→滴加淀粉溶液蓝色;结论:原溶液中一定含有I2A项中O3、Cl2、NO2等都能使品红溶液褪色;B项中H2S、CxHy、HCHO都可出现此现象;C项中浓HNO3等也有此现象。题组二气体的检验D选项实验内容结论A某物质的水溶液能使红色石蕊试纸变蓝该物质一定是氨气B某气体能使湿润的淀粉KI试纸变蓝该气体一定是氧化性气体C苯与溴水混合,溴水褪色苯中含碳碳双键D某物质燃烧后的产物既能使白色硫酸铜粉末变蓝,又能使澄清的石灰水变浑浊该物质一定是碳氢化合物5.根据如表所示实验内容得出的结论正确的是()题组二气体的检验BA项,只要是碱性溶液均可使红色石蕊试纸变蓝,不一定是氨气的水溶液;B项,能使湿润的淀粉KI试纸变蓝的气体一定是氧化性气体,如NO2、溴蒸气等;C项,苯与溴水混合,溴水褪色,是萃取过程,不是加成反应;D项只能说明该物质中可能含有C、H或S、H,既可能为碳氢化合物,也可能为碳氢氧化合物,还可能为硫氢化合物。6.能鉴别MgI2、AgNO3、Na2CO3、NaAl(OH)4四种溶液的试剂是()A.HNO3B.KOHC.BaCl2D.NaClO本题考查物质的鉴别。HNO3氧化I-生成棕色的碘,与Na2CO3反应产生无色的CO2气体,与NaAlO2反应先生成白色沉淀然后溶解,现象均不同。题组三物质的鉴别A7.下列各组物质的无色溶液,不用其他试剂即可鉴别的是()①KOHNa2SO4AlCl3②NaHCO3Ba(OH)2H2SO4③盐酸NaAl(OH)4NaHSO4④Ca(OH)2Na2CO3BaCl2A.①②B.②③C.①③④D.①②④题组三物质的鉴别A①中KOH和AlCl3互滴现象不同,另一种是Na2SO4,可以鉴别;②中H2SO4和NaHCO3反应生成气体,且二者和Ba(OH)2均生成白色沉淀,BaCO3遇H2SO4又能产生气体;③中盐酸、NaHSO4分别与NaAlO2反应的现象相同;④中Ca(OH)2、BaCl2分别与Na2CO3反应现象相同,无法区分开Ca(OH)2与BaCl2。8.(双选)下列各组溶液,不用任何其他试剂就能鉴别的是()A.Na2SO4、H2SO4、AlCl3、BaCl2B.HCl、NaOH、K2SO4、Na2SO4C.NaAlO2、KHCO3、NaCl、NaHSO4D.NaOH、FeCl3、MgCl2、K2SO4D组中的FeCl3溶液呈棕黄色,其他溶液的颜色为无色,故首先鉴别出FeCl3溶液。然后用FeCl3溶液分别与其他三种溶液反应,能产生红褐色沉淀的对应溶液应为NaOH溶液;而MgCl2溶液、K2SO4溶液与FeCl3溶液不发生反应。最后用NaOH溶液来鉴别出MgCl2溶液(产生白色沉淀)和K2SO4溶液(无现象),整个检验过程中发生反应的离子方程式为:Fe3++3OH-===Fe(OH)3↓(红褐色),Mg2++2OH-===Mg(OH)2↓(白色)。其余三组中的各溶液,由于都是无色溶液,无法从外观上加以区别,一般均采用“互滴,A中Na2SO4和H2SO4无法鉴别。B中溶液两两互滴均无明显现象。C中溶液两两互滴,当NaAlO2与NaHSO4滴加顺序不同时现象也不同,可鉴别出NaAlO2和NaHSO4,然后用NaHSO4鉴别开。题组三物质的鉴别CD1.(高考重庆卷)下列实验可实现鉴别目的的是()A.用KOH溶液鉴别SO3(g)和SO2B.用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2C.用CO2鉴别NaAlO2溶液和CH3COONa溶液D.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液题组三物质的鉴别CKOH与SO2和SO3均反应,但无明显现象,不能区分,A项错误;NO2与Br2均具有氧化性,都能使湿润的碘化钾淀粉试纸变蓝,无法区分,B项错误;向NaAlO2溶液中通入CO2发生反应AlO-2+CO2+2H2O===Al(OH)3↓+HCO-3,生成沉淀,醋酸钠与CO2不反应,C项正确;BaCl2溶液与AgNO3、K2SO4分别产生AgCl、BaSO4白色沉淀,无法区分,D项错误。题组三物质的鉴别2.(2014·高考浙江卷)雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH+4、Mg2+、Al3+、SO2-4、NO-3、Cl-。某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下的实验:题组三物质的鉴别B已知:3NO-3+8Al+5OH-+2H2O――→△3NH3↑+8AlO-2根据以上的实验操作与现象,该同学得出的结论不正确的是()A.试样中肯定存在NH+4、Mg2+、SO2-4和NO-3B.试样中一定不含Al3+C.试样中可能存在Na+、Cl-D.该雾霾中可能存在NaNO3、NH4Cl和MgSO4试样加过量Ba(OH)2加热产生的气体1遇湿润红色石蕊试纸显蓝色证明试样中有NH+4;沉淀1加入H+,沉淀部分溶解,说明试样中含Mg2+和SO2-4;根据溶液2的反应和已知信息可知样品中含NO-3;由题目给定的实验不能确定Na+、Cl-、Al3+是否存在。3.(高考海南卷)下列鉴别方法不可行的是()A.用水鉴别乙醇、甲苯和溴苯B.用燃烧法鉴别乙醇、苯和四氯化碳C.用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯D.用酸性高锰酸钾溶液鉴别苯、环已烯和环已烷乙醇溶于水,甲苯浮于水面,溴苯沉在水底,A对;乙醇、苯燃烧火焰有明显差别,而四氯化碳不燃烧,B对;乙醇溶于碳酸钠,乙酸与碳酸钠反应产生气泡,乙酸乙酯浮于溶液表面,C对;酸性高锰酸钾不能氧化苯和环己烷,D错。题组三物质的鉴别D4.(高考江苏卷)下列依据相关实验得出的结论正确的是()A.向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液B.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液C.将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯D.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+能使澄清石灰水变浑浊的可以是CO2也可以是SO2,所以该溶液也可能是亚硫酸盐溶液,A错误;焰色反应火焰呈黄色,该溶液除了钠的盐溶液可以是NaOH溶液,B错误;一种气体使溴水褪色,可以是乙烯,也可以是其他的气态烯烃和气态炔烃,还可以是具有还原性的气体如SO2等,C错误。题组三物质的鉴别D考点二物质的分离与提纯一、组装物质分离提纯的装置1.常规实验装置方法装置条件说明过滤不溶性固体和液体的分离(1)操作中注意____________



 三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
本文标题:物质的检验、分离和提纯课件
链接地址:https://www.777doc.com/doc-5388646 .html